فهرس المحتوى
تحولات المادة
تُعتبر تحولات المادة من الأسسِ في فهمِ عالمِنا الفيزيائي، وهي تتعلق بتغيّرِ حالةِ المادة من صلبةٍ إلى سائلةٍ أو غازيةٍ، أو العكسِ.
فما هو المسببُ الأساسيُّ لهذهِ التحولات؟
إنها الطاقةُ المُختزنةُ في الأجسام، والتي تُعرّفُ بالطاقةِ الكامنة. لا تُختفيِ الطاقةُ الكامنةُ، بل تتحولُ من شكلٍ إلى آخر، ومن جسمٍ إلى آخر. [١]
الذوبان
عندما تُسخّنُ المادةَ الصلبةَ، فإنّ ذراتها تُصبحُ أكثر حركةٍ بسبب اكتسابِها للطاقةِ الحركيّةِ. تُصبح الروابطُ بينَ الذراتِ أضعفَ، مما يؤدي إلى تحولِها من حالةٍ صلبةٍ إلى حالةٍ سائلةٍ.
تُعرفُ هذهِ العمليةُ باسمِ “الذوبان”.
التجمّد
على النقيضِ من ذلك، فإنّ خفضَ درجةِ حرارةِ المادةِ السائلةِ يُؤدي إلى تقليلِ طاقتهاِ الحركيّة. تُصبحُ ذراتُ المادةِ السائلةِ أبطأَ حركةً،
وتُصبح الروابطُ بينَها أقوى.
ينتجُ عن هذهِ العمليةِ تحولُ المادةِ من الحالةِ السائلةِ إلى الحالةِ الصلبةِ،
وهو ما يُعرفُ باسمِ “التجمّد”.
التبخّر
يُعرّفُ “التبخّر” بأنهِ تحولُ المادةِ من الحالةِ السائلةِ إلى الحالةِ الغازيةِ. يحدثُ هذا عندَ رفعِ درجةِ حرارةِ المادةِ إلى درجةِ الغليان،
وهي الدرجةُ التي تُصبحُ فيها ذراتُ المادةِ متحركةً للغايةِ لدرجةِ أنّها تُصبحُ حرةً في الهواءِ.
التكثيف
تُعرّفُ “التكثيف” بأنهاِ عمليةُ تحويلِ المادةِ من الحالةِ الغازيةِ إلى الحالةِ السائلةِ.
تحدثُ هذهِ العمليةُ عندَ تطبيقِ الضغطِ على المادةِ الغازيةِ، مما يُؤدي إلى تباطؤِ حركتهاِ وتقاربِها.
التسامي
تُعرّفُ “التسامي” بأنهاِ تحولُ المادةِ الصلبةِ إلى غازيةٍ، دون المرورِ بالحالةِ السائلة.
تحدثُ هذهِ العمليةُ عندما تكونُ طاقةُ الذراتِ الحركيّةُ أكبرَ من الضغطِ المُطبقِ عليها. [١]
الترسيب
يُعرّفُ “الترسيب” بأنهِ تحولُ المادةِ من غازيةٍ إلى صلبةٍ دون المرورِ بالحالةِ السائلة.
مثالٌ على ذلكِ هو تحولُ بخارِ الماءِ إلى صقيعٍ في درجاتِ الحرارةِ المنخفضة. [١]
حالات المادة الفيزيائيّة
تُعرّفُ المادةُ بشكلٍ عامٍ بأنهاِ أيُّ شيءٍ يشغلُ حيزًا ويمتلكُ كتلةً. تتألفُ جميعُ الموادِ من ذراتٍ وجزيئاتٍ تُربطُ فيما بينها روابط.
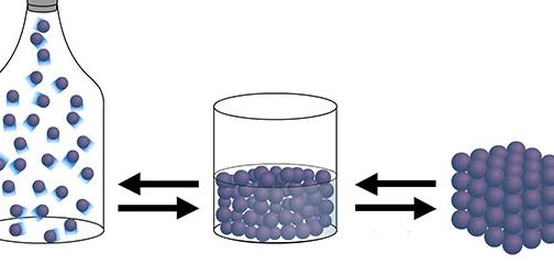
تُقسمُ الموادُ تبعًا لترابطِ الذراتِ وترتيبهاِ واقترابِها من بعضها البعضِ إلى ثلاثةِ أقسامِ رئيسيّةٍ: الموادُ الصلبةُ، السائلةُ، والغازيةُ.
تتمتازُ الموادُ الصلبةُ بروابطِ ذراتِها القويّةِ واقترابِها من بعضِها، مما يُجعلهاِ محافظةً على حجمهاِ وشكلهاِ.
أما الموادُ السائلةُ فتكونُ الروابطُ أقلُّ قوّةً، مما يسمحُ لها بتغييرِ شكلهاِ مع الحفاظِ على حجمهاِ.
بينما تمتلكُ ذراتُ الموادِ الغازيةِ روابطٍ أقلّ تُصعبُ عليهاِ الحفاظُ على كلٍّّ من شكلهاِ وحجمهاِ.
كشفتِ الدراساتُ الحديثةُ عن حالةٍ رابعةٍ للمادةِ تُدعىِ “البلازما”.
تُشبهُ البلازماُ الغازاتِ في عدمِ حفاظهاِ على شكلهاِ وحجمهاِ،
إلا أنّها تُغيّرُ من شحنتهاِ الكهربائيّةِ أيضًا. [٣]
المراجع
- Mary Bagley (11-4-2016), “Matter: Definition & the Five States of Matter”, www.livescience.com, Retrieved 16-12-2018. Edited.
- “Fundamentals of Phase Transitions”, chem.libretexts.org, 25-6-2017, Retrieved 16-12-2018. Edited.
- Anne Marie Helmenstine (31-1-2018), “What Are the States of Matter?”, www.thoughtco.com. Edited.