فهرس المحتوى
- قوانين الغازات
- قانون الغاز المثالي
- قانون بويل
- قانون شارل
- قانون غاي – لوساك
- قانون أفوجادرو
- القانون العالم للغازات
- أمثلة على قوانين الغازات
- المراجع
قوانين الغازات
تُعدّ قوانين الغازات مجموعة من القواعد التي تصف سلوك الغازات في ظل ظروف معينة. تم تطوير هذه القوانين من قبل العلماء في أواخر القرن الثامن عشر، وهي تُركز على العلاقة بين العوامل المختلفة التي تؤثر على سلوك الغازات، مثل:
- الحجم: يُشير إلى المساحة التي يشغلها الغاز.
- الضغط: هو القوة التي يمارسها الغاز على جدران الوعاء الذي يحتويه.
- درجة الحرارة: هي مقياس لمتوسط طاقة حركة جزيئات الغاز.
- كمية المادة: تُعبر عن عدد مولات الغاز الموجودة.
قانون الغاز المثالي
يُعرّف قانون الغاز المثالي بأنه قانون يُصف سلوك غاز افتراضي يُسمى “الغاز المثالي”. في هذا الغاز، يُفترض أن جميع التصادمات بين ذرات الغاز أو جزيئاته مرنة تمامًا، وأنّ لا توجد أي قوى تفاعل بين جزيئات الغاز. يمكن تخيل هذا الغاز كحزمة من الجزيئات التي تتصادم بشكل عشوائي دون أي تفاعل فيما بينها.
يُربط قانون الغاز المثالي جميع العوامل التي تؤثر على الغاز بواسطة المعادلة الرياضية التالية:
P × V = n × R × T
حيث:
- P: الضغط، ويُقاس بوحدة ضغط جوي (atm).
- V: حجم الغاز، ويُقاس بوحدة لتر (L).
- n: عدد مولات الغاز، ويُقاس بوحدة مول (mol).
- R: ثابت الغاز العام، يساوي 0.0821 (L × atm) / (mol × K).
- T: درجة حرارة الغاز، ويُقاس بوحدة كلفن (K).
قانون بويل
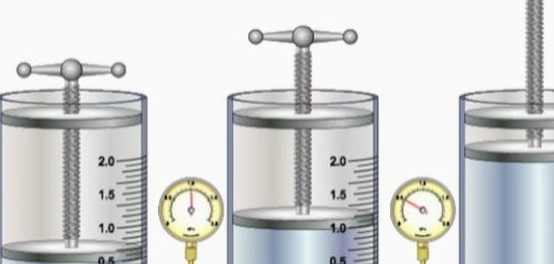
يُصف قانون بويل العلاقة بين ضغط الغاز وحجمه عند ثبات درجة الحرارة. صاغ العالم روبرت بويل هذا القانون، والذي ينص على أنّ ضغط كمية معينة من الغاز يتناسب عكسيًا مع حجم هذا الغاز عند ثبات درجة الحرارة.
يمكن تمثيل قانون بويل بالمعادلة الرياضية التالية:
p × V = c
أو عند مقارنة غازين:
p1 × V1 = p2 × V2
حيث:
- V: حجم الغاز، ويُقاس بوحدة لتر (L).
- p: ضغط الغاز، ويُقاس بوحدة ضغط جوي (atm).
- C: ثابت يعتمد على نوع الغاز ودرجة الحرارة، ووحدته باسكال × متر مكعب (Pa × m3).
قانون شارل
يُربط قانون شارل حجم الغاز المثالي بدرجة حرارته عند ثبات الضغط. ينص قانون شارل على أنّ حجم الغاز المثالي يتناسب طرديًا مع درجة حرارته المطلقة عند ثبوت الضغط. اكتُشفت هذه العلاقة عام 1787 م من قبل العالم جاك شارل.
يمكن تمثيل قانون شارل بالمعادلة الرياضية التالية:
V/T = k
أو عند مقارنة نوعين من الغاز أو حل مسائل تتعلق بنفس الغاز مع تغير الحجم أو درجة الحرارة:
V1/ T1 = V2/ T2
حيث:
- V: حجم الغاز، ويُقاس بوحدة لتر (L).
- T: درجة حرارة الغاز، ويُقاس بوحدة كلفن (K).
- k: ثابت، وقيمته تعتمد على نوع الغاز، ووحدته لتر/كلفن (L/K).
قانون غاي – لوساك
ينص قانون غاي – لوساك على أنّ ضغط الغاز يتناسب طرديًا مع درجة حرارته المطلقة عند ثبات الحجم. صاغ قانون غاي- لوساك الكيميائي الفرنسي جوزيف غاي لوساك في عام 1808 م.
يمكن تمثيل قانون غاي- لوساك بالمعادلة الرياضية التالية:
P / T = k
حيث:
- P: ضغط الغاز، ويُقاس بوحدة باسكال (Pa).
- T: درجة حرارة الغاز، ويُقاس بوحدة كلفن (K).
- k: ثابت، وتختلف قيمته بحسب نوع الغاز ودرجة حرارته، ووحدته باسكال/كلفن (Pa/K).
قانون أفوجادرو
ينص قانون أفوجادرو على أنّ حجم أي غاز يتناسب طرديًا مع عدد جزيئاته عند ثبات الضغط ودرجة الحرارة. يُقاس عدد الجزيئات بالمول. كلما زادت كمية الغاز، يزداد حجمه.
يمكن تمثيل قانون أفوجادرو بالمعادلة الرياضية التالية:
V = k × n
أو عند مقارنة نوعين من الغاز:
V1/n1 = V2/n2
حيث:
- V: حجم الغاز، ويُقاس بوحدة لتر (L).
- k: عدد جزيئات الغاز، ويُقاس بالمول (mol).
- n: ثابت يعتمد على نوع الغاز، ووحدته لتر × مول (L × mol).
القانون العالم للغازات
يُعرف القانون العام للغازات المثالية بأنه قانون يُجمع بين كل من قانون بويل، وقانون شارل، وقانون غاي – لوساك، وقانون أفوجادرو في علاقة رياضية واحدة تصف العلاقة بين الضغط، والحجم، ودرجة الحرارة، وعدد مولات الغاز.
يمكن تمثيل القانون العام للغازات بالمعادلة الرياضية التالية:
P × V = n × R × T
حيث:
- P: ضغط الغاز، ويُقاس بوحدة باسكال (Pa).
- V: حجم الغاز، ويُقاس بوحدة لتر (L).
- n: عدد مولات الغاز، ويُقاس بوحدة مول (mol).
- R: ثابت الغاز العام، يساوي 0.0821 (L × atm) / (mol × K).
- T: درجة حرارة الغاز، ويُقاس بوحدة كلفن (K).
أمثلة على قوانين الغازات
فيما يلي بعض الأمثلة على تطبيقات قوانين الغازات لحل مسائل مختلفة:
حساب الحجم النهائي للغاز
ما هو الحجم النهائي (V2) لعينة من غاز حجمها الابتدائي (V1) يساوي 650 سم3 عند 25 درجة سيليزية (°C) إذا سخنت إلى 400 درجة سيليزية (°C) مع ثبات الضغط؟
الحل:
باستخدام قانون شارل:
V1/ T1 = V2/ T2
مع تحويل درجات الحرارة من سيليزية إلى كلفن:
650 / (25 + 273) = V2/ (400 + 273)
650/ (298) = (V2 / (673)
V2 = 650 (673 / 298)
V2 = 1,468 سم3.
تحويل الحجم إلى لتر:
V2 = 0.002 لتر (L)
حساب عدد مولات الغاز
احسب عدد مولات الهيدروجين الموجودة في 18 لتر (L) من الغاز عند ضغط قدره 70 سم Hg، ودرجة حرارة 27 درجة سيليزية (°C) علمًا أن (R = 0.0821 L. atm/K . mol).
الحل:
باستخدام قانون الغاز المثالي:
P × V = n × R × T
مع تحويل الوحدات حسب النظام العالمي:
(70/67) × 18 = n × 0.0821 × (27 + 273)
n = ((70/67) × 18)/(0.0821 × (27 + 273))
n = 0.673 مول (mol)
حساب الحجم
ما هو حجم الوعاء اللازم لاحتواء 0.0459 مول (mol) من غاز النيتروجين N2 في الظروف المعيارية علمًا أن قيمة الثابت k =22.4؟
الحل:
باستخدام قانون أفوجادرو:
V = k × n
V = 0.0459 × 22.4 لتر (L)
V = 1.3 لتر (L)
حساب حجم الغاز
إذا كانت 4 لتر (L) من غاز معين تحتوي على 0.960 مول (mol) من جزيئات الغاز، فإذا زادت كمية الغاز إلى 1.8 مول (mol)، فما هو الحجم الجديد الناتج من الغاز عند ثبوت الضغط ودرجة الحرارة؟
الحل:
باستخدام قانون أفوجادرو:
V1/n1 = V2/n2
4 /0.96 = V2/ 1.8
V2 = (4 × 1.8)/0.96
V2 = 7.5 لتر (L)
حساب حجم الغاز
عينة من غاز مثالي، إذا كان حجمه (5 لتر) تحت ضغط مقداره (15 atm)، فاحسب حجم هذا الغاز إذا علمت أن ضغطه أصبح (3 atm)، باعتبار درجة الحرارة ثابتة؟
الحل:
باستخدام قانون بويل:
p1 × V1 = p2 × V2
(15 × 5) = (3 × V2)
V2 = (15 × 5)/3
V2 = 25 لتر (L)
حساب عدد المولات
احسب عدد مولات الهيدروجين الموجودة في 18 لتر (L) من الغاز عند ضغط مقداره 70 سم Hg، ودرجة حرارة 27 درجة سيليزية (°C)، علماً أن الثابت R له يساوي 0.0821.
الحل:
باستخدام قانون الغاز المثالي:
PV = n RT
n = PV/RT
مع تحويل الوحدات حسب النظام العالمي:
n = (70 × 18/7)/(0.0821 × (27 + 273))
n = 0.0673 مول (mol)
ملاحظة: يجب الانتباه إلى تحويل درجة الحرارة من سيليزية إلى كلفن.
المراجع
جميع المعلومات المذكورة في هذه المقالة مستمدة من مصادر موثوقة، مثل:
- https://byjus.com/chemistry/combined-gas-law/
- https://hyperphysics.phy-astr.gsu.edu/hbase/kinetic/idegas.html
- https://courses.lumenlearning.com/boundless-chemistry/chapter/relating-pressure-volume-amount-and-temperature-the-ideal-gas-law/
- https://www.britannica.com/science/Boyles-law
- https://www.nasa.gov/mission_pages/sunearth/science/boyle.html
- https://www.scientificamerican.com/article/what-is-charles-law/
- https://www.mocomi.com/what-is-charles-law/
- https://byjus.com/chemistry/gay-lussacs-law/
- https://letstalkscience.ca/educational-resources/science-fair-project-ideas/avogadros-law
- https://courses.lumenlearning.com/boundless-chemistry/chapter/avogadros-law-volume-and-amount/
- https://www.toppr.com/guides/chemistry/states-of-matter/combined-gas-law-formula/