فهرس المحتويات
مقدمة عن الجدول الدوري
الجدول الدوري، المعروف أيضاً بأسماء أخرى مثل جدول مندليف أو الجدول الدوري للعناصر، هو عرض منهجي لجميع العناصر الكيميائية المعروفة في العالم، مُنظمة في شكل جدول. يرجع الفضل في تطوير هذا الجدول إلى الكيميائي ديمتري مندليف في عام 1869. قام مندليف بترتيب العناصر في الجدول بناءً على سلوكها وخصائصها الكيميائية المتشابهة.
كيفية تقسيم الجدول الدوري
يُقسّم الجدول الدوري إلى مجموعات ودورات. يضم الجدول 118 عنصراً كيميائياً. تصنف العناصر من 1 إلى 98 على أنها عناصر طبيعية موجودة في الطبيعة، بينما العناصر من 99 إلى 118 هي عناصر اصطناعية يتم إنتاجها في المختبرات.
أُجريت تعديلات على الجدول الدوري على يد الكيميائي هنري موزلي في عام 1911، حيث أعاد ترتيب العناصر بناءً على عددها الذري. مع مرور الوقت، أُضيفت تعديلات أخرى بعد اكتشاف عناصر جديدة. يُستخدم الجدول الدوري على نطاق واسع في المجالات الأكاديمية الكيميائية لتصنيف وتنظيم العناصر المختلفة وفقاً لخصائصها الكيميائية. كما أنه يستخدم في الكيمياء والفيزياء والهندسة الكيميائية.
تتجلى أهمية الجدول الدوري في استخدامه من قبل العلماء وطلاب الكيمياء لتوفير تفاصيل واضحة حول الخصائص الكيميائية والفيزيائية للعناصر، وكذلك الاختلافات بين المجموعات. فهو أداة أساسية لفهم سلوك العناصر وتفاعلاتها.
السمات الأساسية للجدول الدوري
تتسم عناصر المجموعات الثلاث الأولى في الجدول الدوري بميلها إلى فقد الإلكترونات. بينما تميل عناصر المجموعات الأخرى إلى اكتساب الإلكترونات. هذه الخاصية تحدد إلى حد كبير تفاعلاتها الكيميائية.
تتميز كل دورة في الجدول الدوري بانتهاءها بعنصر خامل. وهذا يعني أن الغلاف الإلكتروني الأخير لهذه العناصر يكون ممتلئاً، مما يجعلها غير قابلة للتفاعل في الظروف العادية.
يمكن تحديد رقم الدورة التي ينتمي إليها العنصر الكيميائي عن طريق حساب عدد الإلكترونات الموجودة في مداره الأخير. هذه المعلومة تساعد في تحديد موقع العنصر في الجدول وبالتالي توقع خصائصه.
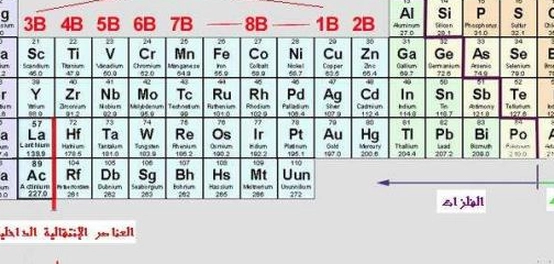
تحتوي أسفل الجدول الدوري على سلسلتي اللانثانيدات والأكتينيدات. تتميز هاتان السلسلتان بطولها الزائد، حيث تحتوي كل منهما على 14 عنصراً كيميائياً. وتنتمي هذه العناصر إلى العناصر الانتقالية.
تصنف العناصر الكيميائية في الجدول الدوري إلى فلزات، ولا فلزات، وأشباه فلزات. لكل فئة من هذه الفئات خصائص مميزة تحدد استخداماتها وتطبيقاتها.
تصنيف العناصر داخل الجدول الدوري
يُبنى الجدول الدوري على شكل دورات ومجموعات، حيث تصنف العناصر الكيميائية وفقاً لخصائصها المتشابهة. يتألف الجدول من ثمانية عشر مجموعة. تتشابه العناصر الموجودة في نفس المجموعة في تركيب غلاف التكافؤ، مما يعني أنها تمتلك نفس عدد الإلكترونات تقريباً، وبالتالي تتشابه في الخواص الكيميائية.
يمتلك الجدول الدوري قدرة فريدة على ترتيب العناصر الكيميائية بدقة عالية. يزداد عدد الطبقات الإلكترونية كلما انتقلنا من سطر إلى آخر، كما يزداد عدد الإلكترونات في الطبقة الخارجية عند الانتقال من عمود إلى آخر. تُرقم المجموعات وفقاً لثلاثة أنظمة: الأرقام العربية، والأرقام الرومانية، والحروف اللاتينية. وقد تم اعتماد الترقيم وفقاً للأرقام العربية من قبل الاتحاد الدولي للكيمياء والكيمياء التطبيقية (IUPAC).